Сучасны PRP: «клінічны PRP»
За апошнія 10 гадоў схема лячэння PRP зведала вялікія змены.Дзякуючы эксперыментальным і клінічным даследаванням мы цяпер лепш разумеем фізіялогію трамбацытаў і іншых клетак.Акрамя таго, некалькі высакаякасных сістэматычных ацэнак, мета-аналізаў і рандомізірованный кантраляваных даследаванняў паказалі эфектыўнасць біятэхналогіі PRP ў многіх галінах медыцыны, уключаючы дэрматалогію, кардыяхірургію, пластычную хірургію, артапедычную хірургію, лячэнне болю, захворванні пазваночніка і спартыўную медыцыну. .
Бягучай характарыстыкай PRP з'яўляецца яго абсалютная канцэнтрацыя трамбацытаў, якая змяняецца ад першапачатковага вызначэння PRP (уключаючы канцэнтрацыю трамбацытаў вышэй зыходнага значэння) да больш чым 1 × 10 6/мкл або прыкладна ў 5 разоў перавышае мінімальную канцэнтрацыю трамбацытаў у трамбацытах з базавая лінія.У шырокім аглядзе Fadadu et al.Былі ацэнены 33 сістэмы і пратаколы PRP.Колькасць трамбацытаў канчатковага прэпарата PRP, вырабленага некаторымі з гэтых сістэм, ніжэй, чым у суцэльнай крыві.Яны паведамілі, што каэфіцыент трамбацытаў PRP павялічыўся да 0,52 пры дапамозе набору з адным кручэннем (Selphyl®).Наадварот, EmCyte Genesis PurePRPII ® з падвойным кручэннем Канцэнтрацыя трамбацытаў, якая ствараецца прыладай, самая высокая (1,6 × 10 6 /мкл).
Відавочна, што метады in vitro і на жывёл не з'яўляюцца ідэальным даследчым асяроддзем для паспяховай трансфармацыі ў клінічную практыку.Падобным чынам даследаванне параўнання прылад не падтрымлівае гэтае рашэнне, таму што яны паказваюць, што канцэнтрацыя трамбацытаў паміж прыладамі PRP моцна адрозніваецца.На шчасце, з дапамогай тэхналогіі і аналізу, заснаванай на пратэёміцы, мы можам палепшыць наша разуменне функцый клетак у PRP, якія ўплываюць на вынікі лячэння.Перш чым дасягнуць кансенсусу па стандартызаваных прэпаратах і складах PRP, PRP павінен прытрымлівацца клінічных рэцэптур PRP, каб спрыяць істотным механізмам аднаўлення тканін і прагрэсіўным клінічным вынікам.
Клінічная формула PRP
У цяперашні час эфектыўны клінічны PRP (C-PRP) характарызуецца як складаны склад аутологичных шматклеткавых кампанентаў у плазме малога аб'ёму, атрыманай з часткі перыферычнай крыві пасля цэнтрыфугавання.Пасля цэнтрыфугавання PRP і яго клеткавыя кампаненты, не звязаныя з трамбацытамі, могуць быць атрыманы з прылады канцэнтрацыі ў адпаведнасці з рознай шчыльнасцю клетак (з якіх шчыльнасць трамбацытаў самая нізкая).
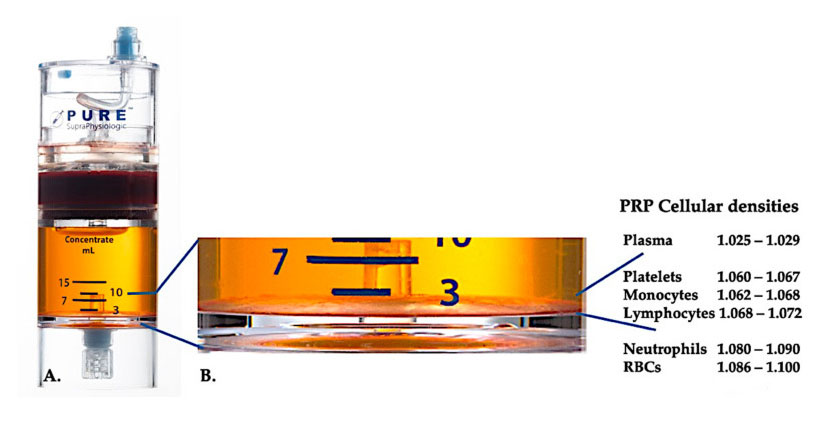
Выкарыстоўвайце PurePRP-SP ® Абсталяванне для падзелу клетак па шчыльнасці (EmCyte Corporation, Форт-Маерс, штат Фларыда, ЗША) выкарыстоўвалася для суцэльнай крыві пасля двух працэдур цэнтрыфугавання.Пасля першага працэсу цэнтрыфугавання кампанент суцэльнай крыві быў падзелены на два асноўныя пласты: завісь трамбацытаў (беднай) плазмы і пласт эрытрацытаў.У А другі этап цэнтрыфугавання завершаны.Фактычны аб'ём PRP можа быць выняты для прымянення пацыентам.Павелічэнне ў B паказвае, што існуе арганізаваны шматкампанентны карычневы пласт асядання эрытрацытаў (прадстаўлены сіняй лініяй) у ніжняй частцы абсталявання, які змяшчае высокія канцэнтрацыі трамбацытаў, манацытаў і лімфацытаў у залежнасці ад градыенту шчыльнасці.У гэтым прыкладзе, у адпаведнасці з пратаколам падрыхтоўкі C-PRP з нізкім утрыманнем нейтрофілов, будзе экстрагаваны мінімальны працэнт нейтрофілов (<0,3%) і эрытрацытаў (<0,1%).
Тромбоцитарные гранулы
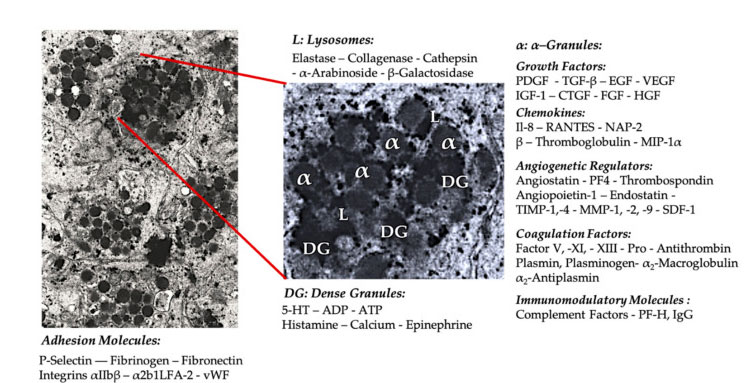
У раннім клінічным прымяненні PRP α-гранулы з'яўляюцца найбольш часта згадванай унутранай структурай трамбацытаў, таму што яны ўтрымліваюць фактары згортвання крыві, вялікую колькасць PDGF і ангіягенных рэгулятараў, але маюць невялікую тромбогенную функцыю.Іншыя фактары ўключаюць у сябе менш вядомыя хемокины і кампаненты цітокіны, такія як фактар трамбацытаў 4 (PF4), претромбоцитарный асноўны бялок, P-селектин (актыватар интегрина) і хемокин RANTES (рэгулюецца актывацыяй, экспрессирующей нармальныя Т-клеткі і, як мяркуецца, вылучаючы).Агульная функцыя гэтых спецыфічных кампанентаў гранул трамбацытаў - прыцягваць і актываваць іншыя імунныя клеткі або выклікаць запаленне эндотелиальных клетак.
Шчыльныя крупчастыя кампаненты, такія як АДФ, серотонін, полифосфат, гістамін і адрэналін, больш няяўна выкарыстоўваюцца ў якасці рэгулятараў актывацыі трамбацытаў і тромбаўтварэння.Самае галоўнае, што многія з гэтых элементаў выконваюць функцыю мадыфікацыі імунных клетак.АДФ трамбацытаў распазнаецца рэцэптарам P2Y12ADP на дендрытных клетках (ДК), што павялічвае эндацытоз антыгена.DC (антыгенпрэзентуючая клетка) вельмі важная для ініцыяцыі імуннага адказу Т-клетак і кантролю ахоўнага імуннага адказу, які звязвае прыроджаную імунную сістэму і адаптыўную імунную сістэму.Акрамя таго, аденозинтрифосфат трамбацытаў (АТФ) пасылае сігналы праз Т-клеткавы рэцэптар P2X7, што прыводзіць да павелічэння дыферэнцыявання Т-хелперных клетак CD4 у провоспалительные Т-хелперы 17 (Th17).Іншыя кампаненты шчыльных гранул трамбацытаў (такія як глутамат і серотонін) індукуюць міграцыю Т-клетак і павялічваюць дыферэнцыявання манацытаў да ДК адпаведна.У PRP гэтыя імунамадулятары, атрыманыя з шчыльных часціц, моцна ўзбагачаны і выконваюць значныя імунныя функцыі.
Колькасць прамых і ўскосных патэнцыяльных узаемадзеянняў паміж трамбацытамі і іншымі (рэцэптарнымі) клеткамі шырокая.Такім чынам, прымяненне PRP ў мясцовай паталагічнай тканкавай асяроддзі можа выклікаць розныя запаленчыя эфекты.
Канцэнтрацыя трамбацытаў
C-PRP павінен утрымліваць клінічныя дозы канцэнтраваных трамбацытаў для атрымання дабратворнага тэрапеўтычнага эфекту.Трамбацыты ў C-PRP павінны стымуляваць праліферацыі клетак, сінтэз мезенхімальных і нейротрофических фактараў, спрыяць міграцыі хемотаксических клетак і стымуляваць иммунорегуляторную актыўнасць, як паказана на малюнку.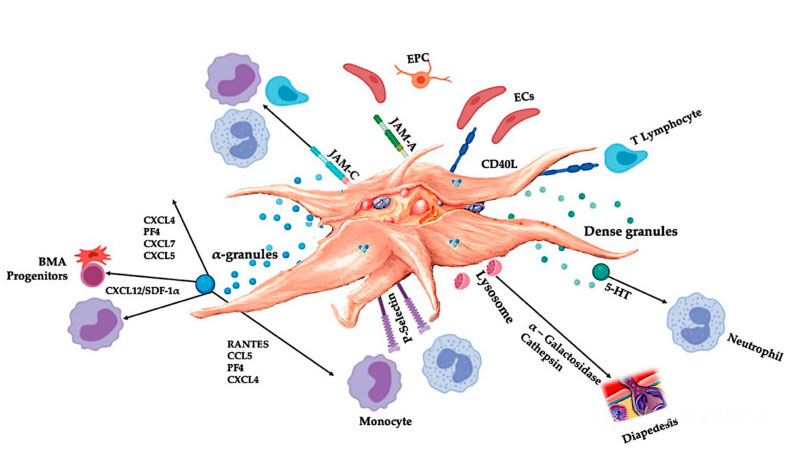
Актываваныя трамбацыты, вызваленне PGF і малекулы адгезіі апасродкуюць розныя клеткавыя ўзаемадзеяння: хемотаксис, клетачную адгезію, міграцыю і клетачную дыферэнцыяцыю, а таксама рэгулююць рэгулятарную дзейнасць імунітэту.Гэтыя ўзаемадзеянні паміж клеткамі трамбацытаў спрыяюць ангіягенезу і актыўнасці запалення і ў канчатковым выніку стымулююць працэс аднаўлення тканін.Скарачэнні: BMA: аспірат касцявога мозгу, EPC: эндотелиальные клеткі-папярэднікі, EC: эндотелиальные клеткі, 5-HT: 5-гидрокситриптамин, RANTES: актываваная рэгуляцыя нармальнай экспрэсіі Т-клетак і меркаванай сакрэцыі, JAM: тып малекулы адгезіі, CD40L: кластар 40 ліганд, SDF-1 α: фактар-1 α, атрыманы з стромальных клетак, CXCL: хемокін (матыў CXC) ліганд, PF4: фактар трамбацытаў 4. Адаптавана з Everts et al.
Маркс быў першым чалавекам, які даказаў, што гаенне костак і мяккіх тканін паляпшаецца, а мінімальная колькасць трамбацытаў складае 1 × 10 6 /мкл. Гэтыя вынікі былі пацверджаны ў даследаванні паяснічнага зрашчэння праз міжпазваночныя адтуліны, калі доза трамбацытаў была больш, чым 1,3 × Пры 106 трамбацытаў/мкл гэта даследаванне прадэманстравала большае зліццё.Акрамя таго, Giusti і соавт.Выяўлена 1,5 × Механізм аднаўлення тканін пры дозе 109 патрабуе трамбацытаў/мл для індукцыі функцыянальнага ангіягенезу праз актыўнасць эндотелиальных клетак.У апошнім даследаванні больш высокія канцэнтрацыі зніжалі патэнцыял ангіягенезу трамбацытаў у фалікулах і вакол іх.Акрамя таго, больш раннія дадзеныя паказалі, што доза PRP таксама будзе ўплываць на вынікі лячэння.Такім чынам, каб істотна індукаваць рэакцыю ангіягенезу і стымуляваць клеткавую праліферацыю і клеткавую міграцыю, C-PRP павінен утрымліваць не менш за 7,5 у 5-мл флаконе для лячэння PRP × 10 9 можа даставіць трамбацыты.
У дадатак да залежнасці ад дозы, уплыў PRP на актыўнасць клетак, здаецца, моцна залежыць ад часу.Сафі і інш.Гэтыя вынікі сведчаць аб тым, што кароткачасовае ўздзеянне лизатов трамбацытаў чалавека можа стымуляваць праліферацыі касцяных клетак і хемотаксис.Наадварот, доўгатэрміновае ўздзеянне PRP прывядзе да зніжэння ўзроўню шчолачнай фасфатазы і адукацыі мінералаў.
Эрытрацыт
Эрытрацыты адказваюць за транспарціроўку кіслароду да тканін і перанос вуглякіслага газу з тканін у лёгкія.Яны не маюць ядра і складаюцца з малекул гема, якія звязваюцца з вавёркамі.Кампаненты жалеза і гема ў эрытрацытах спрыяюць спалучэнню кіслароду і вуглякіслага газу.Як правіла, жыццёвы цыкл эрытрацытаў складае каля 120 дзён.Яны выдаляюцца з кровазвароту макрафагамі ў працэсе, які называецца старэннем эрытрацытаў.Эрытрацыты ва ўзорах PRP могуць пашкоджвацца ва ўмовах зруху (напрыклад, аперацыя з крывацёкам суцэльнай крыві, імунны працэс, акісляльны стрэс або неадэкватная схема канцэнтрацыі PRP).Такім чынам, клеткавая мембрана эрытрацытаў раскладаецца і вызваляе таксічны гемаглабін (Hb), вымераны свабодным гемаглабінам плазмы (PFH), гемам і жалезам.].PFH і прадукты яго дэградацыі (гем і жалеза) разам прыводзяць да шкоднага і цітотоксіческой ўздзеяння на тканіны, што прыводзіць да акісляльнага стрэсу, страты аксіду азоту, актывацыі шляхоў запалення і імунасупрэсіі.Гэтыя эфекты ў канчатковым выніку прывядуць да дысфункцыі мікрацыркуляцыі, мясцовага звужэння сасудаў і пашкоджання сасудаў, а таксама да сур'ёзнага пашкоджання тканін.
Самае важнае, што калі эрытрацыты, якія змяшчаюць C-PRP, дастаўляюцца ў тканіну, гэта выкліча мясцовую рэакцыю, званую эрыптозам, якая выкліча вызваленне эфектыўнага цітокіны і інгібітара міграцыі макрафагаў.Гэты цітокіны душыць міграцыю манацытаў і макрофагов.Ён падае моцныя провоспалительные сігналы навакольным тканінам, інгібіруе міграцыю ствалавых клетак і праліферацыі фібрабластаў і прыводзіць да значнай лакальнай дысфункцыі клетак.Такім чынам, важна абмежаваць забруджванне эрытрацытаў у прэпаратах PRP.Акрамя таго, ніколі не была вызначана роля эрытрацытаў у рэгенерацыі тканін.Адэкватнае цэнтрыфугаванне C-PRP і працэс падрыхтоўкі звычайна памяншаюць або нават ліквідуюць прысутнасць эрытрацытаў, пазбягаючы такім чынам негатыўных наступстваў гемолізу і полицитемии.
Лейкацыты ў С-ПРП
Наяўнасць лейкацытаў у прэпаратах PRP залежыць ад лячэбнага абсталявання і схемы падрыхтоўкі.У абсталяванні PRP на аснове плазмы лейкацыты цалкам ліквідуюцца;Тым не менш, лейкацыты былі значна сканцэнтраваны ў падрыхтоўцы PRP карычневага пласта ссядання эрытрацытаў.Дзякуючы сваім імунным механізмам і механізмам абароны гаспадара, лейкацыты моцна ўплываюць на ўнутраную біялогію вострых і хранічных станаў тканін.Гэтыя функцыі будуць разгледжаны ніжэй.Такім чынам, наяўнасць спецыфічных лейкацытаў у C-PRP можа выклікаць значныя клеткавыя і тканкавыя эфекты.Дакладней, у розных сістэмах ссядання эрытрацытаў у карычнева-жоўтым слоі PRP выкарыстоўваюцца розныя схемы падрыхтоўкі, што стварае розную долю нейтрофілов, лімфацытаў і манацытаў у PRP.Эозінофілы і базофилы нельга вымераць у прэпаратах PRP, таму што іх клеткавыя мембраны занадта далікатныя, каб супрацьстаяць цэнтрабежным сілам апрацоўкі.
Нейтрофілов
Нейтрофілов з'яўляюцца важнымі лейкацытамі ў многіх шляхах гаення.Гэтыя шляхі спалучаюцца з антымікробнымі вавёркамі, якія прысутнічаюць у трамбацытах, утвараючы шчыльны бар'ер супраць інвазівных патагенаў.Існаванне нейтрофілов вызначаецца ў адпаведнасці з мішэнню лячэння C-PRP.Павышэнне ўзроўню запалення тканін можа спатрэбіцца пры лячэнні хранічнай раны PRP-біятэрапіяй або пры ўжыванні, накіраваным на рост або гаенне костак.Важна адзначыць, што ў некалькіх мадэлях былі знойдзены дадатковыя функцыі нейтрофілов, што падкрэслівае іх ролю ў ангиогенезе і аднаўленні тканін.Аднак нейтрофілы таксама могуць выклікаць шкодныя наступствы, таму яны не падыходзяць для некаторых ужыванняў.Чжоу і Ван даказалі, што выкарыстанне PRP, багатага нейтрофілов, можа прывесці да павелічэння суадносін калагена III тыпу і калагена I тыпу, такім чынам, пагаршаючы фіброз і зніжаючы трываласць сухажылляў.Іншыя шкодныя характарыстыкі, апасродкаваныя нейтрофілов, - гэта вызваленне запаленчых цітокінаў і металапратэіназ матрыцы (ММР), якія могуць спрыяць запаленню і катабалізму пры нанясенні на тканіны.
Лейкаманацыт
У C-PRP аднаядзерныя Т- і В-лімфацыты больш канцэнтраваныя, чым любыя іншыя лейкацыты.Яны цесна звязаны з клеткавым цітотоксіческой адаптыўным імунітэтам.Лімфацыты могуць выклікаць клеткавыя рэакцыі для барацьбы з інфекцыяй і адаптацыі да захопнікаў.Акрамя таго, цітокіны Т-лімфацытаў (інтэрферон-γ [IFN-γ] і інтэрлейкін-4 (IL-4) узмацняюць палярызацыю макрофагов. Verassar et al. Даказана, што звычайныя Т-лімфацыты могуць ускосна спрыяць гаенню тканін у мышынай мадэлі, рэгулюючы дыферэнцыявання манацытаў і макрофагов.
Манацыт - мультипотентная рэпарацыйная клетка
У залежнасці ад выкарыстоўванай прылады падрыхтоўкі PRP, манацыты могуць выступаць або не быць у бутэльцы для лячэння PRP.На жаль, іх працаздольнасць і здольнасць да рэгенерацыі рэдка абмяркоўваюцца ў літаратуры.Такім чынам, мала ўвагі надаецца манацытаў у метадзе падрыхтоўкі або канчатковай формуле.Група манацытаў гетэрагенная, паходзіць з клетак-папярэднікаў у касцяным мозгу і транспартуецца ў перыферычныя тканіны праз шлях крывятворных ствалавых клетак у адпаведнасці са стымуляцыяй мікраасяроддзя.Падчас гамеастазу і запалення цыркулюючыя манацыты пакідаюць крывацёк і прыцягваюцца да пашкоджаных або дэградаваных тканін.Яны могуць дзейнічаць як макрафагі (M Φ) эфектарныя клеткі або клеткі-папярэднікі.Манацыты, макрафагі і дендрытныя клеткі ўяўляюць сабой монануклеарную фагацытарную сістэму (MPS). Тыповай асаблівасцю MPS з'яўляецца пластычнасць схемы экспрэсіі генаў і функцыянальнае перакрыцце паміж гэтымі тыпамі клетак.У дэгенераваных тканінах рэзідэнтныя макрафагі, фактары росту мясцовага дзеяння, провоспалительные цітокіны, апоптотические або некратычныя клеткі і мікробныя прадукты ініцыююць манацыты дыферэнцавацца ў групы клетак MPS.Выкажам здагадку, што калі C-PRP, які змяшчае манацыты з высокім ураджаем, уводзяць у мясцовае мікраасяроддзе захворвання, манацыты, хутчэй за ўсё, дыферэнцуюцца ў M Φ, каб выклікаць сур'ёзныя змены клетак.
Ад манацытаў да M Φ У працэсе трансфармацыі, спецыфічны M Φ фенатып.За апошнія дзесяць гадоў была распрацавана мадэль, якая аб'ядноўвае M Φ. Складаны механізм актывацыі апісваецца як палярызацыя двух супрацьлеглых станаў: M Φ фенатыпу 1 (M Φ 1, класічная актывацыя) і M Φ фенатыпу 2 (M Φ 2, альтэрнатыўная актывацыя).M Φ 1 характарызуецца запаленчай сакрэцыяй цітокіны (IFN-γ) і аксіду азоту для стварэння эфектыўнага механізму знішчэння патагенаў.M Φ Фенатып таксама вырабляе фактар росту эндатэлю сасудаў (VEGF) і фактар росту фібрабластаў (FGF).M Φ Фенатып складаецца з супрацьзапаленчых клетак з высокім фагацытозам.M Φ 2 Вырабляюць кампаненты пазаклеткавага матрікса, ангіягенез і хемокіны, а таксама інтэрлейкін 10 (IL-10).У дадатак да абароны ад патагенаў, M Φ Ён таксама можа паменшыць запаленне і спрыяць аднаўленню тканін.Варта адзначыць, што M Φ 2 быў падзелены на M in vitro Φ 2a、M Φ 2b і M Φ 2. Гэта залежыць ад стымулу.Пераклад in vivo гэтых падтыпаў цяжкі, таму што тканіна можа ўтрымліваць змешаныя M Φ групы.Цікава, што зыходзячы з мясцовых сігналаў навакольнага асяроддзя і ўзроўню IL-4, провоспалительный M Φ 1 можа быць пераўтвораны, каб спрыяць аднаўленню M Φ 2。 З гэтых даных разумна выказаць здагадку, што існуюць высокія канцэнтрацыі манацытаў і прэпаратаў M Φ C-PRP могуць спрыяць лепшаму аднаўленню тканін, таму што яны валодаюць супрацьзапаленчым аднаўленнем тканін і здольнасцю перадачы клетачнага сігналу.
Пераблытанае вызначэнне фракцыі лейкацытаў у PRP
Наяўнасць лейкацытаў у флаконах для лячэння PRP залежыць ад прылады падрыхтоўкі PRP і можа істотна адрознівацца.Існуе шмат спрэчак наконт існавання лейкацытаў і іх укладу ў розныя суб-PRP прадукты (такія як PRGF, P-PRP, LP-PRP, LR-PRP, P-PRF і L-PRF) У нядаўнім аглядзе шэсць рандомізірованный У кантраляваных выпрабаваннях (узровень доказнасці 1) і трох проспективных параўнальных даследаваннях (узровень доказнасці 2) удзельнічалі 1055 пацыентаў, што паказвае на аднолькавую бяспеку LR-PRP і LP-PRP.Аўтар прыйшоў да высновы, што пабочная рэакцыя PRP не можа быць непасрэдна звязана з канцэнтрацыяй лейкацытаў.У іншым даследаванні LR-PRP не змяніў запаленчы інтэрлейкін (IL-1) пры ОА каленнага сустава β、 IL-6, IL-8 і IL-17).Гэтыя вынікі пацвярджаюць меркаванне, што роля лейкацытаў у біялагічнай актыўнасці PRP in vivo можа зыходзіць ад перакрыжаваных перашкод паміж трамбацытамі і лейкацытамі.Гэта ўзаемадзеянне можа спрыяць біясінтэзу іншых фактараў (напрыклад, кіслароду), якія могуць кампенсаваць або спрыяць рэгрэсіі запалення.Пасля першаснага вызвалення запаленчых малекул (арахідонавай кіслаты, лейкатрыену і простагландыну) з актываваных трамбацытаў вызваляецца ліпаксірод А4, каб прадухіліць актывацыю нейтрофілов.Менавіта ў гэтым асяроддзі M Φ фенатып з M Φ 1 пераключаецца на M Φ 2. Акрамя таго, з'яўляецца ўсё больш доказаў таго, што цыркулюючыя аднаядзерныя клеткі могуць дыферэнцавацца ў розныя нефагацытарныя тыпы клетак дзякуючы сваёй плюрыпатэнтнасці.
Тып PRP будзе ўплываць на культуру MSC.У параўнанні з чыстымі ўзорамі PRP або PPP, LR-PRP можа выклікаць значна большую праліферацыю МСК касцявога мозгу (BMMSC) з больш хуткім вызваленнем і лепшай біялагічнай актыўнасцю PGF.Усе гэтыя характарыстыкі спрыяюць даданню манацытаў у бутэлечку для лячэння PRP і прызнанню іх імунамадулюючых здольнасцей і патэнцыялу дыферэнцыявання.
Прыроджаная і адаптыўная імунная рэгуляцыя PRP
Самая вядомая фізіялагічная функцыя трамбацытаў - кантраляваць крывацёк.Яны назапашваюцца ў месцы пашкоджання тканін і пашкоджаных сасудаў.Гэтыя падзеі выкліканы экспрэсіяй интегринов і селектинов, якія стымулююць адгезію і агрэгацыю трамбацытаў.Пашкоджаны эндатэлю яшчэ больш пагаршае гэты працэс, а адкрыты калаген і іншыя вавёркі субэндотелиального матрікса спрыяюць глыбокай актывацыі трамбацытаў.У гэтых выпадках даказаная важная роля ўзаемадзеяння фактару фон Виллебранда (vWF) і глікапратэіна (GP), асабліва GP-Ib.Пасля актывацыі трамбацытаў α-、 шчыльныя, лізасомы і Т-гранулы рэгулююць экзацытоз і вызваляюць іх змесціва ў пазаклеткавае асяроддзе.
Малекула адгезіі трамбацытаў
Каб лепш зразумець ролю PRP у запаленчых тканінах і трамбацытаў у імуннай рэакцыі, мы павінны зразумець, як розныя паверхневыя рэцэптары трамбацытаў (интегрины) і малекулы адгезіі (JAM) і ўзаемадзеянне клетак могуць ініцыяваць важныя працэсы ў прыроджаным і адаптыўным імунітэце.
Інтэгрыны - гэта малекулы адгезіі клетачнай паверхні, якія знаходзяцца ў розных тыпах клетак і экспрэсаваныя ў вялікіх колькасцях на трамбацытах.Інтэгрыны ўключаюць a5b1, a6b1, a2b1 LFA-2, (GPIa/IIa) і aIIbb3 (GPIIb/IIIa).Звычайна яны існуюць у статычным стане з нізкім сродствам.Пасля актывацыі яны пераходзяць у стан высокага сродства да звязвання ліганда.Интегрины выконваюць розныя функцыі на трамбацыты і ўдзельнічаюць ва ўзаемадзеянні трамбацытаў з некалькімі тыпамі лейкацытаў, эндотелиальными клеткамі і пазаклеткавай матрікса.Акрамя таго, комплекс GP-Ib-V-IX экспрессируется на мембране трамбацытаў і з'яўляецца асноўным рэцэптарам для звязвання з von vWF.Гэта ўзаемадзеянне апасродкуе першапачатковы кантакт паміж трамбацытамі і аголенымі субэндотелиальными структурамі.Интегрин трамбацытаў і комплекс ГП звязаны з рознымі запаленчымі працэсамі і гуляюць важную ролю ў адукацыі тромбоцітарные-лейкоцітарный комплексу.У прыватнасці, интегрин aIIbb3 неабходны для адукацыі стабільнага комплексу шляхам аб'яднання фібрынаген з рэцэптарам антыгена макрофагов 1 (Mac-1) на нейтрофілов.
Трамбацыты, нейтрофілов і эндотелиальные клеткі сасудаў экспрессируют спецыфічныя малекулы клеткавай адгезіі, званыя селектином.Ва ўмовах запалення трамбацыты экспрессируют Р-селектин і нейтрофілов L-селектин.Пасля актывацыі трамбацытаў Р-селектин можа звязвацца з лигандом PSGL-1, які існуе на нейтрофілов і манацытах.Акрамя таго, звязванне PSGL-1 ініцыюе ўнутрыклеткавую каскадную рэакцыю сігналу, якая актывуе нейтрофілов праз нейтрофілов інтэграмін Mac-1 і антыген 1, звязаны з функцыяй лімфацытаў (LFA-1).Актываваны Mac-1 звязваецца з GPIb або GPIIb/IIIa на трамбацытаў праз фібрынаген, такім чынам стабілізуючы ўзаемадзеянне паміж нейтрофілов і трамбацытаў.Акрамя таго, актываваны LFA-1 можа спалучацца з малекулай міжклеткавай адгезіі трамбацытаў 2 для далейшай стабілізацыі комплексу нейтрофілов і трамбацытаў для спрыяння доўгатэрміновай адгезіі з клеткамі.
Трамбацыты і лейкацыты гуляюць ключавую ролю ў прыроджаных і адаптыўных імунных рэакцыях
Цела можа распазнаваць іншародныя цела і пашкоджаныя тканіны пры вострых або хранічных захворваннях, каб ініцыяваць каскадную рэакцыю гаення ран і шлях запалення.Прыроджаная і адаптыўная імунная сістэма абараняе гаспадара ад інфекцыі, і лейкацыты гуляюць важную ролю ў перакрыцці паміж дзвюма сістэмамі.У прыватнасці, манацыты, макрафагі, нейтрофілы і натуральныя клеткі-кілеры гуляюць ключавую ролю ў прыроджанай сістэме, у той час як лімфацыты і іх падгрупы гуляюць аналагічную ролю ў адаптыўнай імуннай сістэме.
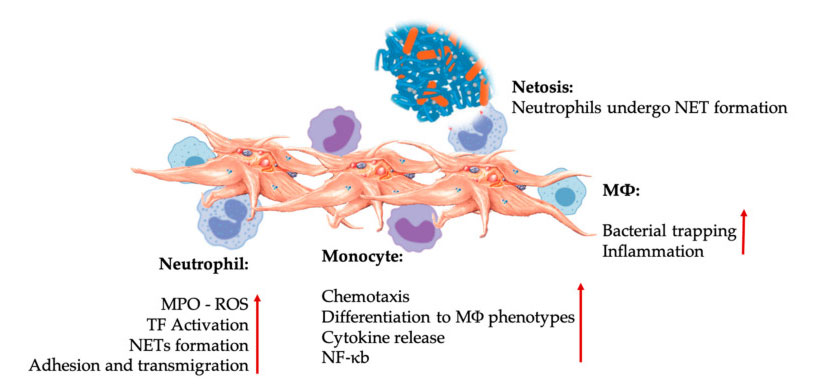
Узаемадзеянне трамбацытаў і лейкацытаў ва ўзаемадзеянні прыроджаных імунных клетак.Трамбацыты ўзаемадзейнічаюць з нейтрофілов і манацытамі, і, нарэшце, з M Φ Узаемадзейнічаюць, карэктуюць і павялічваюць іх эффекторные функцыі.Гэтыя ўзаемадзеянні трамбацытаў і лейкацытаў прыводзяць да запалення з дапамогай розных механізмаў, уключаючы НЕТоз.Скарачэнні: MPO: миелопероксидаза, ROS: актыўныя формы кіслароду, TF: тканкавы фактар, NET: пазаклеткавая пастка нейтрофілов, NF-κ B: ядзерны фактар каппа B, M Φ: Макрафагі.
Прыроджаная імунная сістэма
Роля прыроджанай імуннай сістэмы заключаецца ў неспецыфічнай ідэнтыфікацыі інвазівных мікраарганізмаў або фрагментаў тканін і стымуляванні іх ачышчэння.Калі пэўныя малекулярныя структуры, якія называюцца рэцэптарамі распазнання патэрнаў экспрэсіі на паверхні (PRR), спалучаюцца з малекулярнымі патэрнамі, звязанымі з патагенамі, і малекулярнымі патэрнамі, звязанымі з пашкоджаннямі, актывуецца прыроджаная імунная сістэма.Існуе шмат відаў PRR, у тым ліку Toll-падобны рэцэптар (TLR) і RIG-1-падобны рэцэптар (RLR).Гэтыя рэцэптары могуць актываваць асноўны фактар транскрыпцыі каппа B (NF-κ B). Ён таксама рэгулюе некалькі аспектаў прыроджанага і адаптыўнага імуннага адказу.Цікава, што трамбацыты таксама экспрэсуюць на сваёй паверхні і ў цытаплазме розныя імунарэгулятарныя малекулы рэцэптараў, такія як P-селектын, трансмембранны бялок CD40-ліганд (CD40L), цітокіны (напрыклад, IL-1 β, TGF- β) і трамбацытаспецыфічны TLR. Такім чынам, трамбацыты могуць ўзаемадзейнічаць з рознымі імуннымі клеткамі.
Узаемадзеянне трамбацытаў і белых клетак у прыроджаным імунітэце
Калі трамбацыты трапляюць або ўрываюцца ў крывацёк або тканіны, трамбацыты з'яўляюцца адной з клетак, якія першымі выяўляюць пашкоджанне эндатэлю і мікробныя ўзбуджальнікі.Агрэгацыя трамбацытаў і садзейнічанне вызваленню агоністом трамбацытаў АДФ, трамбіна і vWF, што прыводзіць да актывацыі трамбацытаў і экспрэсіі хемокиновых рэцэптараў трамбацытаў C, CC, CXC і CX3C, такім чынам, выклікаючы трамбацыты ў інфікаваным месцы або пашкоджанні.
Прыроджаная імунная сістэма генетычна прадвызначана выяўляць захопнікаў, такіх як вірусы, бактэрыі, паразіты і таксіны, або раны і раны ў тканінах.Гэта неспецыфічная сістэма, таму што любы ўзбуджальнік будзе ідэнтыфікаваны як чужародны або неўласны і хутка знойдзены.Прыроджаная імунная сістэма абапіраецца на набор бялкоў і фагацытаў, якія распазнаюць добра захаваныя характарыстыкі патагенаў і хутка актывуюць імунны адказ, каб дапамагчы ліквідаваць захопнікаў, нават калі гаспадар ніколі раней не падвяргаўся ўздзеянню пэўных патагенаў.
Нейтрофілов, манацытаў і дендрітных клетак з'яўляюцца найбольш распаўсюджанымі клеткамі прыроджанага імунітэту ў крыві.Іх прыцягненне неабходна для адэкватнага ранняга імуннага адказу.Калі PRP выкарыстоўваецца ў рэгенератыўнай медыцыне, узаемадзеянне трамбацытаў і лейкацытаў рэгулюе запаленне, гаенне ран і аднаўленне тканін.TLR-4 на трамбацытах стымулюе ўзаемадзеянне трамбацытаў і нейтрофілов, якое рэгулюе так званы акісляльны выбух лейкацытаў, рэгулюючы вызваленне актыўных формаў кіслароду (АФК) і миелопероксидазы (МПО) з нейтрофілов.Акрамя таго, узаемадзеянне паміж трамбацытаў-нейтрофілов і дэгрануляцыяй нейтрофілов прыводзіць да адукацыі нейтрофілов-пазаклеткавых пастак (NET).NET складаюцца з ядра нейтрофілов і іншага ўнутрыклеткавага змесціва нейтрофілов, якое можа захопліваць бактэрыі і забіваць іх праз NETosis.Адукацыя NET з'яўляецца важным механізмам знішчэння нейтрофілов.
Пасля актывацыі трамбацытаў манацыты могуць міграваць у хворыя і дэгенератыўныя тканіны, дзе яны ажыццяўляюць адгезійную дзейнасць і вылучаюць малекулы запалення, якія могуць змяніць хемотаксис і пратэялітычныя ўласцівасці.Акрамя таго, трамбацыты могуць індукаваць актывацыю NF-κ B манацытаў для рэгулявання эфектарнай функцыі манацытаў, якая з'яўляецца ключавым медыятарам запаленчай рэакцыі і актывацыі і дыферэнцыявання імунных клетак.Трамбацыты дадаткова спрыяюць эндагеннаму акісляльнаму выбуху манацытаў, каб спрыяць знішчэнню фагацытарных патагенаў.Вызваленне MPO апасродкавана прамым узаемадзеяннем паміж CD40L-MAC-1 трамбацытаў і манацытаў.Цікава, што калі Р-селектын актывуе трамбацыты пры вострых і хранічных запаленчых станах тканін, атрыманыя з трамбацытаў хемокины PF4, RANTES, IL-1β і CXCL-12 могуць прадухіліць спантанны апоптоз манацытаў, але спрыяюць іх дыферэнцыяцыі ў макрафагі.
Адаптыўная імунная сістэма
Пасля таго, як неспецыфічная прыроджаная імунная сістэма распазнае мікробнае або тканкавае пашкоджанне, спецыфічная адаптыўная імунная сістэма бярэ на сябе.Адаптыўныя сістэмы ўключаюць антыген-звязваючыя В-лімфацыты (В-клеткі) і звычайныя Т-лімфацыты (Treg), якія каардынуюць ачышчэнне патагенаў.Т-клеткі можна груба падзяліць на Т-клеткі-хелперы (Th-клеткі) і цітотоксіческой Т-клеткі (Тс-клеткі, таксама вядомыя як Т-клеткі-кілеры).Клеткі Th таксама дзеляцца на клеткі Th1, Th2 і Th17, якія выконваюць ключавыя функцыі пры запаленні.Th-клеткі могуць вылучаць провоспалительные цітокіны (напрыклад, IFN-γ、 TNF-β) і некалькі інтэрлейкінаў (напрыклад, IL-17). Яны асабліва эфектыўныя ў прадухіленні ўнутрыклеткавай віруснай і бактэрыяльнай інфекцыі. Th-клеткі стымулююць праліферацыю і дыферэнцыяцыю клетак, якія ўдзельнічаюць у імунная рэакцыя Тс-клеткі - эфектарныя клеткі, якія могуць ліквідаваць мэтавыя ўнутрыклеткавыя і пазаклеткавыя мікраарганізмы і клеткі.
Цікава, што клеткі Th2 вырабляюць IL-4 і ўплываюць на M Φ палярызацыю, M Φ накіраваную рэгенерацыю M Φ 2 фенатып, у той час як IFN- γ M Φ змяняецца на запаленчы M Φ фенатып 1, які залежыць ад дозы і часу цітокіны.Пасля актывацыі IL-4 M Φ 2 прымушае клеткі Treg дыферэнцавацца ў клеткі Th2, а затым вырабляе дадатковы IL-4 (пятля станоўчай зваротнай сувязі).Th клеткі ператвараюць M Φ Фенатып накіраваны на рэгенератыўны фенатып у адказ на біялагічныя агенты тканкавага паходжання.Гэты механізм заснаваны на доказах таго, што Th-клеткі гуляюць значную ролю ў кантролі запалення і аднаўленні тканін.
Узаемадзеянне трамбацытаў і белых клетак у адаптыўным імунітэце
Адаптыўная імунная сістэма выкарыстоўвае антыген-спецыфічныя рэцэптары і запамінае патагены, з якімі раней сутыкаліся, і знішчае іх, калі пасля сутыкаецца з гаспадаром.Аднак гэтыя адаптыўныя імунныя рэакцыі развіваліся павольна.Коніас і інш.Гэта паказвае, што трамбацытаў кампанент спрыяе ўспрыманню рызыкі і аднаўленню тканін, і што ўзаемадзеянне паміж трамбацытамі і лейкацытамі спрыяе актывацыі адаптыўнага імуннага адказу.
Падчас адаптыўнага імуннага адказу трамбацыты спрыяюць рэакцыі манацытаў і макрофагов праз паспяванне клетак DC і NK, што прыводзіць да спецыфічных рэакцый Т-клетак і В-клетак.Такім чынам, кампаненты гранул трамбацытаў непасрэдна ўплываюць на адаптыўны імунітэт шляхам экспрэсіі CD40L, малекулы, якая важная для рэгуляцыі адаптыўнага імуннага адказу.Трамбацыты праз CD40L не толькі гуляюць ролю ў прэзентацыі антыгена, але і ўплываюць на рэакцыю Т-клетак.Лю і інш.Было выяўлена, што трамбацыты складаным чынам рэгулююць адказ Т-клетак CD4.Такая дыферэнцыяльная рэгуляцыя падмностваў Т-клетак CD4 азначае, што трамбацыты спрыяюць рэагаванню Т-клетак CD4 на раздражняльнікі запалення, ствараючы такім чынам моцныя провоспалительные і супрацьзапаленчыя рэакцыі.
Трамбацыты таксама рэгулююць апасродкаваную В-клеткамі адаптыўную рэакцыю на мікробныя патагены.Добра вядома, што CD40L на актываваных Т-клетках CD4 будзе запускаць CD40 У-клетак, забяспечваючы другі сігнал, неабходны для залежнай ад Т-клетак актывацыі В-лімфацытаў, наступнай канверсіі аллотипа і дыферэнцыявання і праліферацыі В-клетак.У цэлым вынікі ясна паказваюць розныя функцыі трамбацытаў у адаптыўным імунітэце, паказваючы на тое, што трамбацыты звязваюць узаемадзеянне паміж Т-клеткамі і В-клеткамі праз CD40-CD40L, такім чынам узмацняючы залежны ад Т-клетак адказ У-клетак.Акрамя таго, трамбацыты багатыя рэцэптарамі клетачнай паверхні, якія могуць спрыяць актывацыі трамбацытаў і вызваляць вялікую колькасць запаленчых і біялагічна актыўных малекул, якія захоўваюцца ў розных часціцах трамбацытаў, уплываючы такім чынам на прыроджаны і адаптыўны імунны адказ.
Пашырэнне ролі трамбацытаў серотоніна ў PRP
Серотонін (5-гидрокситриптамин, 5-НТ) мае пэўную ключавую ролю ў цэнтральнай нервовай сістэме (ЦНС), уключаючы талерантнасць да болю.Мяркуецца, што большая частка чалавечага 5-HT выпрацоўваецца ў страўнікава-кішачным тракце, а затым праз кровазварот, дзе ён паглынаецца трамбацытамі праз транспарцёр зваротнага захопу серотоніна і захоўваецца ў шчыльных часціцах пры высокай канцэнтрацыі (65 ммоль/л).5-HT - гэта вядомы нейрамедыятар і гармон, які дапамагае рэгуляваць розныя нервова-псіхалагічныя працэсы ў ЦНС (цэнтральны 5-HT).Тым не менш, большая частка 5-HT існуе па-за ЦНС (перыферычны 5-HT), і ён удзельнічае ў рэгуляцыі сістэмных і клеткавых біялагічных функцый розных сістэм органаў, у тым ліку сардэчна-сасудзістай сістэмы, лёгкіх, страўнікава-кішачнага гасцінца, мочеполовой сістэмы і функцыянальных сістэм трамбацытаў.5-HT мае залежны ад канцэнтрацыі метабалізм розных тыпаў клетак, уключаючы адыпацыты, эпітэліяльныя клеткі і лейкацыты.Перыферычны 5-HT таксама з'яўляецца магутным імунным мадулятарам, які можа стымуляваць або інгібіраваць запаленне і ўплываць на розныя імунныя клеткі праз свой спецыфічны рэцэптар 5-HT (5HTR).
Паракринный і аутокринный механізм ГТ
Дзейнасць 5-HT апасродкавана яго ўзаемадзеяннем з 5HTR, якое з'яўляецца суперсямействам з сямі членаў (5-HT 1 - 7) і па меншай меры 14 розных падтыпаў рэцэптараў, у тым ліку нядаўна адкрытага члена 5-HT 7, яго перыферыйных і функцыя ў барацьбе з болем.У працэсе дэгрануляцыі трамбацытаў актываваныя трамбацыты вылучаюць вялікую колькасць 5-HT, які паходзіць з трамбацытаў, які можа спрыяць скарачэнню сасудаў і стымуляваць актывацыю прылеглых трамбацытаў і лімфацытаў праз экспрэсію 5-HTR на эндотелиальных клетках, гладкомышечных клетках і імунныя клеткі.Пакала і інш.Было вывучана митотическое дзеянне 5-НТ на клеткі эндатэлю сасудаў, а таксама вызначаны патэнцыял стымулявання росту пашкоджаных крывяносных сасудаў шляхам стымуляцыі ангіягенезу.Не зусім ясна, як гэтыя працэсы рэгулююцца, але яны могуць уключаць дыферэнцыяльныя двухбаковыя сігнальныя шляхі ў мікрасхеме тканіны для рэгулявання функцый клетак эндатэлю сасудаў і гладкомышечных клетак, фібрабластаў і імунных клетак праз спецыфічныя рэцэптары 5-НТ на гэтых клетках. .Была апісана аутокринная функцыя трамбацытаў 5-HT пасля актывацыі трамбацытаў [REF].Вызваленне 5-HT ўзмацняе актывацыю трамбацытаў і вярбоўку цыркулююць трамбацытаў, што прыводзіць да актывацыі сігнальных каскадных рэакцый і вышэйшых эфектараў, якія падтрымліваюць рэактыўнасць трамбацытаў.
Імунамадулюючыя 5-HT эфект
Усё больш доказаў паказвае, што серотонін можа гуляць пэўную ролю ў розных 5HTR як імунамадулятар.Згодна з 5HTR, які экспрэсуецца ў розных лейкацытах, якія ўдзельнічаюць у запаленчай рэакцыі, 5-HT, атрыманы з трамбацытаў, дзейнічае як імунны рэгулятар як у прыроджанай, так і ў адаптыўнай імуннай сістэме.5-HT можа стымуляваць праліферацыю Treg і рэгуляваць функцыі B-клетак, натуральных клетак-кілераў і нейтрофілов шляхам прыцягнення DC і манацытаў да агменю запалення.Нядаўнія даследаванні паказалі, што трамбацытаў 5-НТ можа рэгуляваць функцыю імунных клетак пры пэўных умовах.Такім чынам, выкарыстанне C-PRP, калі канцэнтрацыя трамбацытаў перавышае 1 × 10 6/мкл, можа значна дапамагчы транспартаваць канцэнтрацыю 5-НТ, атрыманую з буйных трамбацытаў, у тканіны.У мікраасяроддзі, якое характарызуецца запаленчымі кампанентамі, PRP можа ўзаемадзейнічаць з некалькімі імуннымі клеткамі, якія гуляюць ключавую ролю ў гэтых паталогіях, што можа паўплываць на клінічныя вынікі.
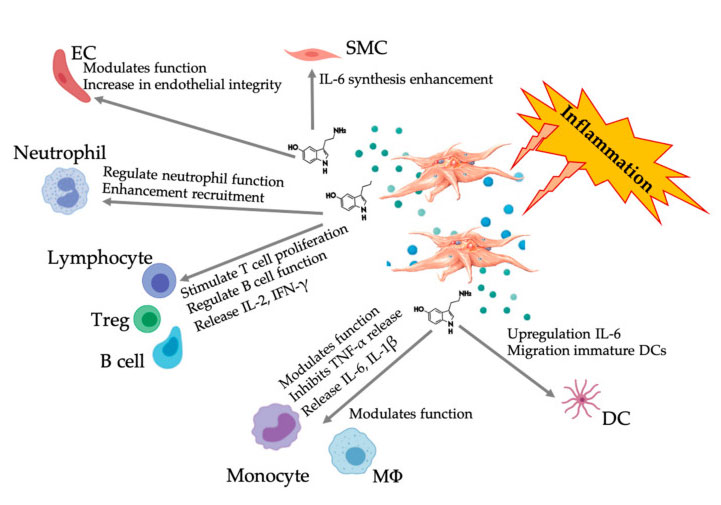
Малюнак, які адлюстроўвае шматбаковую рэакцыю 5-НТ пасля актывацыі запаленчых трамбацытаў PRP.Пасля актывацыі трамбацытаў, трамбацыты вызваляюць свае гранулы, у тым ліку 5-HT ў шчыльных гранулах, які аказвае шырокі спектр дыферэнцыяльнага ўздзеяння на розныя імунныя клеткі, эндотелиальные клеткі і гладкомышечные клеткі.Скарачэнні: SMC: гладкомышечные клеткі, EC: эндотелиальные клеткі, Treg: звычайныя Т-лімфацыты, M Φ: макрафагі, DC: дендрытныя клеткі, IL: інтэрлейкін, IFN-γ: інтэрферон γ。 Мадыфікавана і адаптавана з Everts et al.і Халл і інш.
Абязбольвальнае дзеянне PRP
Актываваныя трамбацыты вызваляць шмат провоспалительных і супрацьзапаленчых медыятараў, якія могуць не толькі выклікаць боль, але і паменшыць запаленне і боль.Пасля прымянення тыповая дынаміка трамбацытаў PRP змяняе мікраасяроддзе перад аднаўленнем і рэгенерацыяй тканін з дапамогай розных складаных шляхоў, звязаных з анабалізмам і катабалізмам, праліферацыяй клетак, дыферэнцыяцыяй і рэгуляцыяй ствалавых клетак.Гэтыя характарыстыкі PRP прыводзяць да прымянення PRP пры розных клінічных паталагічных станах, звычайна звязаных з хранічнай болем (напрыклад, пры спартыўных траўмах, артапедычных захворваннях, захворваннях пазваночніка і складаных хранічных ранах), хоць дакладны механізм да канца не вызначаны.
У 2008 годзе Evertz і соавт.Гэта першае рандомізірованное кантраляванае даследаванне, у якім паведамляецца аб абязбольвальным эфекце прэпарата PRP, які атрымліваецца з карычневага пласта аўтолагічнай хуткасці ссядання эрытрацытаў і актывуецца аўтолагічным трамбінам пасля аперацыі на плячы.Яны адзначылі значнае зніжэнне балаў па візуальнай аналагавай шкале, выкарыстанне анальгетыкаў на аснове апіоідаў і больш паспяховую пасляаперацыйную рэабілітацыю.Характэрна, што яны адлюстроўваюць абязбольвальнае дзеянне актываваных трамбацытаў і мяркуюць механізм вызвалення трамбацытамі 5-НТ.Карацей кажучы, у свежапрыгатаваным PRP трамбацыты знаходзяцца ў стане спакою.Пасля прамой або ўскоснай актывацыі трамбацытаў (тканкавы фактар) трамбацыты змяняюць форму і вырабляюць дастаткова ілжывых, каб спрыяць агрэгацыі трамбацытаў.Затым яны вызваляюць ўнутрыклеткавых α- і шчыльныя часціцы.Тканіна, апрацаваная актываваным PRP, будзе захоплена PGF, цітокіны і іншымі лізасомамі трамбацытаў.Дакладней, калі шчыльныя часціцы вызваляюць сваё змесціва, яны вылучаюць вялікую колькасць 5-НТ, які рэгулюе боль.Пры C-PRP канцэнтрацыя трамбацытаў у 5-7 разоў вышэй, чым у перыферычнай крыві.Такім чынам, вызваленне 5-НТ з трамбацытаў астранамічнае.Цікава, што Sprott і соавт.У справаздачы адзначаецца, што боль значна палягчаецца пасля іглаўколвання і прыпякання, канцэнтрацыя 5-HT, атрыманага з трамбацытаў, значна зніжаецца, а затым павышаецца ўзровень 5-HT у плазме.
У перыферычнай частцы трамбацыты, гладкія клеткі і эндотелиальные клеткі будуць вылучаць эндагенны 5-HT падчас пашкоджання тканін або хірургічнай траўмы.Цікава, што мноства рэцэптараў 5-HT нейронаў былі выяўленыя ў перыферычнай вобласці, што пацвердзіла, што 5-HT можа перашкаджаць ноцицептивной перадачы ў перыферычнай вобласці.Гэтыя даследаванні паказваюць, што 5-HT можа ўплываць на ноцицептивную перадачу перыферычных тканін праз рэцэптары 5-HT1, 5-HT2, 5-HT3, 5-HT4 і 5-HT7.
Сістэма 5-HT уяўляе сабой магутную сістэму, якая можа паменшыць і павялічыць ступень болю пасля шкоднай стымуляцыі.Паведамляецца аб цэнтральнай і перыферычнай рэгуляцыі ноцицептивных сігналаў і зменах у сістэме 5-НТ у пацыентаў з хранічнай болем.У апошнія гады вялікая колькасць даследаванняў была сканцэнтравана на ролі 5-НТ і яго адпаведных рэцэптараў у апрацоўцы і рэгуляванні шкоднай інфармацыі, у выніку чаго з'явіліся такія лекі, як селектыўныя інгібітары зваротнага захопу серотоніна (СИОЗС).Гэты прэпарат інгібіруе зваротны захоп серотоніна пресінаптіческой нейронамі пасля вызвалення серотоніна.Гэта ўплывае на працягласць і інтэнсіўнасць сувязі серотоніна і з'яўляецца альтэрнатыўным метадам лячэння хранічнай болю.Неабходныя далейшыя клінічныя даследаванні, каб дакладна зразумець малекулярны механізм рэгуляцыі болю 5-HT, атрыманай з PRP, пры хранічных і дэгенератыўных захворваннях.
Іншыя даныя для вырашэння патэнцыйнага абязбольвальнага эфекту PRP можна атрымаць пасля тэсту на абязбольвальных жывёл.Параўнальныя статыстычныя высновы ў гэтых мадэлях з'яўляюцца складанымі, таму што гэтыя даследаванні ўтрымліваюць занадта шмат зменных.Тым не менш, у некаторых клінічных даследаваннях разглядаліся ноцицептивные і абязбольвальныя эфекты PRP.Некалькі даследаванняў паказалі, што пацыенты, якія атрымліваюць лячэнне ад тэндынозу або разрыву рататарнай абшэўкі, практычна не палягчаюць боль.Наадварот, некалькі іншых даследаванняў паказалі, што PRP можа паменшыць або нават ліквідаваць боль у пацыентаў з дэгенерацыяй сухажылляў, ОА, падэшвеннай фасцыі і іншымі захворваннямі ступні і галенастопа.Канчатковая канцэнтрацыя трамбацытаў і біялагічны клеткавы склад былі вызначаны ў якасці ключавых характарыстык PRP, якія дапамагаюць назіраць стабільны абязбольвальны эфект пасля прымянення PRP.Іншыя зменныя ўключаюць спосаб дастаўкі PRP, тэхналогію прымянення, пратакол актывацыі трамбацытаў, узровень біялагічнай актыўнасці PGF і вызваленых цітокіны, тып тканіны прымянення PRP і тып пашкоджанні.
Характэрна, што Куфлер раскрыў патэнцыял PRP у палягчэнні болю ў пацыентаў з лёгкай і цяжкай хранічнай неўрапатычнай болем, другаснай у сувязі з пашкоджаным нерэгенератыўным нервам.Мэта гэтага даследавання - высветліць, ці можа неўрапатычная боль быць паменшана або сціхла дзякуючы PRP, які спрыяе рэгенерацыі аксона і рэінервацыі мэтавага нерва.Дзіўна, але сярод пацыентаў, якія атрымліваюць лячэнне, неўрапатычная боль усё яшчэ ліквідуецца або палягчаецца па меншай меры праз шэсць гадоў пасля аперацыі.Акрамя таго, усе пацыенты пачалі палягчаць боль на працягу трох тыдняў пасля прымянення PRP.
Нядаўна падобныя абязбольвальныя эфекты PRP назіраліся ў галіне сыходу за пасляаперацыйнымі ранамі і скурай.Цікава, што аўтары паведамілі аб фізіялагічных аспектах раневой болю, звязаных з пашкоджаннем сасудаў і гіпаксіяй скурных тканін.Яны таксама абмеркавалі важнасць ангіягенезу ў аптымізацыі аксігенацыі і дастаўкі пажыўных рэчываў.Іх даследаванне паказала, што ў параўнанні з кантрольнай групай пацыенты, якія атрымлівалі лячэнне PRP, мелі менш болю і значна павялічвалі ангіягенез.Нарэшце, Джохал і яго калегі правялі сістэматычны агляд і мета-аналіз і прыйшлі да высновы, што PRP можа паменшыць боль пасля выкарыстання PRP па артапедычных паказаннях, асабліва ў пацыентаў, якія атрымліваюць лячэнне вонкавага эпікандыліту і ОА каленнага сустава.На жаль, гэта даследаванне не ўдакладняе эфекты лейкацытаў, канцэнтрацыі трамбацытаў або выкарыстання экзагенных актыватараў трамбацытаў, таму што гэтыя зменныя паўплываюць на агульную эфектыўнасць PRP.Аптымальная канцэнтрацыя трамбацытаў PRP для максімальнага палягчэння болю незразумелая.У пацучынай мадэлі тэндынозу канцэнтрацыя трамбацытаў была 1,0 × 10 6 / μ. Пры L боль можа быць цалкам знята, у той час як палягчэнне болю, выкліканае PRP з паловай канцэнтрацыі трамбацытаў, значна зніжаецца.Такім чынам, мы заклікаем праводзіць дадатковыя клінічныя даследаванні для вывучэння анальгетычнага эфекту розных прэпаратаў PRP.
Эфект PRP і ангіягенезу
Прэпараты C-PRP у дакладнай рэгенератыўнай медыцыне дазваляюць дастаўляць біямалекулы, якія выдзяляюцца высокай канцэнтрацыяй трамбацытаў, актываваных у месцах тканін-мішэняў.Такім чынам, былі пачаты розныя каскадныя рэакцыі, якія спрыяюць рэгуляцыі імуннай сістэмы на месцы, запаленчым працэсам і ангіягенезу для садзейнічання гаенню і аднаўленню тканін.
Ангіягенез - гэта дынамічны шматэтапны працэс, які ўключае прарастанне і тканкавыя мікрасасуды з ужо існуючых крывяносных сасудаў.Ангіягенез прагрэсаваў дзякуючы розным біялагічным механізмам, уключаючы міграцыю, праліферацыю, дыферэнцыяцыю і дзяленне эндотелиальных клетак.Гэтыя клеткавыя працэсы з'яўляюцца перадумовамі для адукацыі новых крывяносных сасудаў.Яны важныя для росту існуючых крывяносных сасудаў для аднаўлення крывацёку і падтрымкі высокай метабалічнай актыўнасці аднаўлення і рэгенерацыі тканін.Гэтыя новыя крывяносныя пасудзіны дазваляюць дастаўляць кісларод і пажыўныя рэчывы, а таксама выдаляць пабочныя прадукты з апрацаваных тканін.
Актыўнасць ангиогенеза рэгулюецца стымулюючым ангиогенным фактарам VEGF і анты-ангиогенными фактарамі (напрыклад, ангиостатином і тромбоспондином-1 [TSP-1]).У хворым і пагаршаным мікраасяроддзі (уключаючы нізкае напружанне кіслароду, нізкі рн і высокі ўзровень малочнай кіслаты) мясцовыя ангіягенныя фактары аднаўляюць актыўнасць ангіягенезу.
Некалькі растваральных трамбацытаў асяроддзяў, такіх як асноўны FGF і TGF-β і VEGF, могуць стымуляваць эндотелиальные клеткі да вытворчасці новых крывяносных сасудаў.Landsdown і Fortier паведамілі аб розных выніках, звязаных з PRP кампазіцыяй, у тым ліку внутритромбоцитарных крыніц многіх ангиогенных рэгулятараў.Акрамя таго, яны прыйшлі да высновы, што павышэнне ангіягенезу спрыяе гаенню хваробы MSK у раёнах з дрэннай васкулярызацыяй, такіх як разрыў меніска, пашкоджанне сухажыллі і іншыя вобласці з дрэннай васкулярызацыяй.
Садзейнічанне і анты-ангиогенные ўласцівасці трамбацытаў
За апошнія некалькі дзесяцігоддзяў апублікаваныя даследаванні паказалі, што трамбацыты гуляюць ключавую ролю ў першасным гемастазе, адукацыі тромбаў, вызваленні фактару росту і цітокіны, а таксама рэгуляцыі ангіягенезу як часткі працэсу аднаўлення тканін.Парадаксальна, але гранулы PRP α- утрымліваюць арсенал праангіягенных фактараў росту, антыангіягенных бялкоў і цітокіны (такіх як PF4, інгібітар актыватара плазмінагену-1 і TSP-1), і накіраваны на вызваленне спецыфічных фактараў, якія гуляюць ролю .Роля ў ангіягенезе.Такім чынам, роля PRP ў кантролі рэгуляцыі ангіягенезу можа быць вызначана актывацыяй спецыфічных рэцэптараў клетачнай паверхні, TGF-β, які ініцыіруе праангіягенныя і антыангіягенныя рэакцыі.Здольнасць трамбацытаў ажыццяўляць шлях ангіягенезу была пацверджана пры паталагічным ангіягенезе і пухлінным ангіягенезе.
Ангиогенный фактар росту трамбацытаў і анты-ангиогенный фактар росту, атрыманы з α- і шчыльных і клейкіх малекул.Самае галоўнае, што агульнапрызнана, што агульны эфект трамбацытаў на ангіягенез з'яўляецца проангиогенным і стымулюючым.Чакаецца, што PRP-тэрапія будзе кантраляваць індукцыю ангіягенезу, што будзе спрыяць лячэбнаму эфекту многіх захворванняў, такіх як гаенне ран і аднаўленне тканін.Увядзенне PRP, больш канкрэтна ўвядзенне высокай канцэнтрацыі PGF і іншых цітокіны трамбацытаў, можа індукаваць ангіягенез, ангіягенез і артэрыягенез, паколькі фактар 1а, атрыманы з стромальных клетак, звязваецца з рэцэптарам CXCR4 на эндотелиальных клетках-папярэдніках.Біл і інш.Мяркуюць, што PRP павялічвае ішэмічную неоваскуляризацию, што можа быць звязана са стымуляцыяй ангиогенеза, ангиогенеза і артериогенеза.У іх мадэлі in vitro праліферацыі эндотелиальных клетак і адукацыя капіляраў выклікаліся вялікай колькасцю розных PDG, з якіх VEGF быў асноўным ангиогенным стымулятарам.Іншым важным і істотным фактарам для аднаўлення шляху ангіягенезу з'яўляецца сінэргія паміж некалькімі PGF.Рычардсан і інш.Было даказана, што сінэргічны актыўнасць ангиогенного фактару тромбоцитарного фактару росту-bb (PDGF-BB) і VEGF прывяла да хуткага адукацыі спелай сасудзістай сеткі ў параўнанні з актыўнасцю індывідуальнага фактару росту.Камбінаваны эфект гэтых фактараў быў нядаўна пацверджаны ў даследаванні ўзмацнення цэрэбральнага коллатерального кровазвароту ў мышэй з працяглай гипоперфузией.
Самае галоўнае, што даследаванне in vitro вымярала праліфератыўны эфект эндатэліяльных клетак пупавіннай вены чалавека і розных канцэнтрацый трамбацытаў на выбар прылады падрыхтоўкі PRP і стратэгіі дозы трамбацытаў, і вынікі паказалі, што аптымальная доза трамбацытаў складала 1,5 × 10 6 трамбацытаў/мкм. 50. Для садзейнічання ангіягенезу.Занадта высокая канцэнтрацыя трамбацытаў можа тармазіць працэс ангіягенезу, таму эфект дрэнны.
Старэнне клетак, старэнне і PRP
Старэнне клетак можа быць выклікана рознымі стымуламі.Гэта працэс, пры якім клеткі перастаюць дзяліцца і падвяргаюцца унікальным фенатыпічным зменам, каб прадухіліць неабмежаваны рост пашкоджаных клетак, што гуляе важную ролю ў прафілактыцы рака.У працэсе фізіялагічнага старэння рэплікацыйнае старэнне клетак таксама будзе спрыяць старэнню клетак, і здольнасць МСК да рэгенерацыі будзе зніжана.
Наступствы старэння і старэнне клетак
In vivo многія тыпы клетак старэюць і назапашваюцца ў розных тканінах падчас старэння, сярод якіх ёсць вялікая колькасць старэючых клетак.Здаецца, назапашванне старэючых клетак павялічваецца з узростам, пашкоджаннем імуннай сістэмы, пашкоджаннем тканін або фактарамі, звязанымі са стрэсам.Механізм клеткавага старэння быў ідэнтыфікаваны як патагенны фактар узроставых захворванняў, такіх як астэаартоз, астэапароз і дэгенерацыя міжхрыбеткавага дыска.Разнастайныя раздражняльнікі пагаршаюць старэнне клетак.У адказ сакраторны фенатып, звязаны са старэннем (SASP), будзе вылучаць высокія канцэнтрацыі бялковых клетак і цітокіны.Гэты асаблівы фенатып звязаны са старэннем клетак, у якіх яны вылучаюць высокі ўзровень запаленчых цітокінаў (такіх як IL-1, IL-6, IL-8), фактараў росту (такіх як TGF-β, HGF, VEGF, PDGF), MMP і катепсин.У параўнанні з маладымі людзьмі, было даказана, што SAPS павялічваецца з узростам, таму што стацыянарны працэс разбураецца, што прыводзіць да старэння клетак і зніжэння здольнасці да рэгенерацыі.У прыватнасці, пры захворваннях суставаў і шкілетных цягліц.У сувязі з гэтым старэнне імунітэту лічыцца значным змяненнем спектру сакрэцыі імунных клетак, якое сведчыць аб павышэнні канцэнтрацыі TNF-a, IL-6 і/або IL-1b, што прыводзіць да хранічнага запалення нізкай ступені.Варта адзначыць, што дысфункцыя ствалавых клетак таксама звязана з неклеткавымі аўтаномнымі механізмамі, такімі як старэнне клетак, асабліва выпрацоўка прозапаленчых і антырэгенератыўных фактараў праз SASP.
Наадварот, SASP можа таксама стымуляваць пластычнасць клетак і перапраграмаванне суседніх клетак.Акрамя таго, SASP можа арганізаваць сувязь з рознымі імуннымі медыятарамі і актываваць імунныя клеткі, каб спрыяць ачышчэнню старэючых клетак.Разуменне ролі і функцыі клетак, якія старэюць, будзе спрыяць гаенню і рэканструкцыі тканін МСК цягліц і хранічных ран.
Характэрна, што Ritcka et al.Было праведзена шырокае даследаванне, і была выяўлена асноўная і карысная роля SASP у садзейнічанні пластычнасці клетак і рэгенерацыі тканін, і была ўведзена канцэпцыя часовага лячэння старэючых клетак.Яны асцярожна адзначылі, што старэнне - гэта пераважна карысны і рэгенерацыйны працэс.
Старэнне клетак і патэнцыял PRP
Калі колькасць ствалавых клетак памяншаецца, старэнне будзе ўплываць на працу ствалавых клетак.Сапраўды гэтак жа ў людзей характарыстыкі ствалавых клетак (такія як сухасць, праліферацыя і дыферэнцыяцыя) таксама памяншаюцца з узростам.Ван і Нірмала паведамілі, што старэнне прывядзе да зніжэння характарыстык ствалавых клетак сухажылляў і колькасці рэцэптараў фактару росту.Даследаванне на жывёл паказала, што канцэнтрацыя PDGF у маладых коней была высокай.Яны прыйшлі да высновы, што павелічэнне колькасці рэцэптараў GF і колькасці GF у маладых людзей можа мець лепшы клеткавы адказ на лячэнне PRP, чым у пажылых людзей у маладых людзей.Гэтыя вынікі паказваюць, чаму лячэнне PRP можа быць менш эфектыўным ці нават неэфектыўным у пажылых пацыентаў з меншай колькасцю ствалавых клетак і «дрэннай якасцю».Даказана, што пасля ін'екцыі PRP працэс старэння храстковай тканіны адмяняецца, а перыяд спакою хандрацытаў павялічваецца.Цзя і інш.Ён выкарыстоўваецца для вывучэння фотастарэння скурных фібрабластаў мышэй in vitro з лячэннем PRP і без яго, каб высветліць механізм процідзеяння PGF у гэтай мадэлі.Група PRP прадэманстравала непасрэдны ўплыў на пазаклеткавы матрыкс, павелічэнне калагена тыпу I і зніжэнне сінтэзу металапратэіназ, што паказвае на тое, што PRP можа супрацьстаяць старэнню клетак, а таксама пры дэгенератыўных захворваннях MSK.
У іншым даследаванні PRP выкарыстоўваўся для збору састарэлых ствалавых клетак касцявога мозгу ў старых мышэй.Было ўстаноўлена, што PRP можа аднаўляць розныя функцыі ствалавых клетак у выніку старэння, такія як праліферацыя клетак і фарміраванне калоній, і рэканструяваць маркеры, звязаныя са старэннем клетак.
Нядаўна Оберлор і яго калегі шырока вывучалі ролю старэння клетак у паслабленні рэгенерацыі цягліц і ацанілі PRP і бедную трамбацытамі плазму (PPP) як варыянты біялагічнага лячэння для аднаўлення шкілетных цягліц.Яны меркавалі, што лячэнне PRP або PPP для аднаўлення шкілетных цягліц будзе заснавана на біялагічных фактарах, наладжаных для маркераў спецыфічных клетак SASP і іншых фактараў, якія прыводзяць да развіцця фіброзу.
Разумна меркаваць, што да прымянення PRP мэтанакіраванае старэнне клетак можа палепшыць рэгенерацыйныя характарыстыкі эфектыўнасці біялагічнай апрацоўкі за кошт зніжэння мясцовых фактараў SASP.Было выказана меркаванне, што яшчэ адным варыянтам паляпшэння вынікаў лячэння PRP і PPP для рэгенерацыі шкілетных цягліц з'яўляецца выбарачнае выдаленне старэючых клетак з дапамогай паглынальнікаў старэння.Няма сумненняў у тым, што нядаўнія вынікі даследаванняў уплыву PRP на старэнне і старэнне клетак захапляюць, але яны ўсё яшчэ знаходзяцца ў пачатковай стадыі.Такім чынам, неразумна рабіць якія-небудзь прапановы ў гэты час.
(Змесціва гэтага артыкула перадрукавана, і мы не даем ніякіх відавочных або пэўных гарантый на дакладнасць, надзейнасць або паўнату змесціва, якое змяшчаецца ў гэтым артыкуле, і не нясем адказнасці за меркаванні гэтага артыкула, калі ласка, зразумейце.)
Час публікацыі: 1 сакавіка 2023 г