Канцэпцыя, вядомая сёння як PRP, упершыню з'явілася ў галіне гематалогіі ў 1970-х гадах.Гематолагі ўвялі тэрмін PRP дзесяцігоддзі таму, спрабуючы апісаць плазму, атрыманую з колькасці трамбацытаў вышэй базальных значэнняў у перыферычнай крыві.Больш чым праз дзесяць гадоў PRP быў выкарыстаны ў сківічна-тварнай хірургіі як форма багатага трамбацытамі фібрына (PRF).Змест фібрына ў гэтым вытворным PRP мае вялікае значэнне з-за яго адгезійных і гомеастатычных уласцівасцяў, у той час як PRP валодае ўстойлівымі супрацьзапаленчымі ўласцівасцямі і стымулюе праліферацыі клетак.Нарэшце, прыкладна ў 1990-я гады, PRP стаў папулярным, і ў рэшце рэшт, тэхналогія была перанесена ў іншыя медыцынскія вобласці.З тых часоў гэтая пазітыўная біялогія шырока вывучалася і прымянялася для лячэння розных пашкоджанняў апорна-рухальнага апарата ў прафесійных спартсменаў, што яшчэ больш спрыяла шырокай увазе СМІ.Акрамя эфектыўнасці ў артапедыі і спартыўнай медыцыне, PRP выкарыстоўваецца ў афтальмалогіі, гінекалогіі, уралогіі і кардыялогіі, педыятрыі і пластычнай хірургіі.У апошнія гады дэрматолагі таксама высока ацанілі PRP за яго патэнцыял для лячэння язваў на скуры, рэвізіі рубцоў, рэгенерацыі тканін, амаладжэння скуры і нават выпадзення валасоў.
Улічваючы той факт, што PRP, як вядома, непасрэдна маніпулюе працэсамі гаення і запаленчых працэсаў, лячэбны каскад павінен быць уведзены ў якасці эталона.Працэс гаення дзеліцца на наступныя чатыры этапы: гемастаз;запаленне;праліферацыі клетак і матрыцы, і, нарэшце, рэканструкцыя раны.
1. Гаенне тканін
Актывізуецца каскад гаення тканін, працэс, які прыводзіць да агрэгацыі трамбацытаў, адукацыі тромбаў і развіццю часовага пазаклеткавага матрікса (ECM. Затым трамбацыты прыліпаюць да адкрытых бялкоў калагена і ECM, выклікаючы прысутнасць α-гранул у вызваленні Біялагічна актыўныя малекулы. Трамбацыты ўтрымліваюць розныя біялагічна актыўныя малекулы, у тым ліку фактары росту, хемакіны і цітокіны, а таксама провоспалительные медыятары, такія як простагландыны, цыклін прастаты, гістамін, трамбаксан, серотонін і брадыкінін.
Канчатковы этап працэсу гаення залежыць ад перабудовы раны.Рэканструкцыя тканін жорстка рэгулюецца, каб усталяваць баланс паміж анабалічнымі і катабалічнымі рэакцыямі.Падчас гэтай фазы тромбоцітарные фактар росту (PDGF), трансфармуючы фактар росту (TGF-β) і фибронектин стымулююць праліферацыі і міграцыю фібрабластаў, а таксама сінтэз кампанентаў ECM.Аднак тэрміны паспявання раны шмат у чым залежаць ад цяжару раны, індывідуальных асаблівасцяў і спецыфічнай здольнасці да гаення пашкоджанай тканіны, а некаторыя патафізіялагічныя і метабалічныя фактары могуць уплываць на працэс гаення, напрыклад, ішэмія тканін, гіпаксія, інфекцыя , Дысбаланс фактару росту і нават захворванні, звязаныя з метабалічным сіндромам.
Провоспалительное мікраасяроддзе, якое перашкаджае працэсу гаення.Што ўскладняе сітуацыю, існуе таксама высокая актыўнасць протеазы, якая інгібіруе натуральнае дзеянне фактару росту (GF).У дадатак да мітагенных, ангіягенных і хематаксічных уласцівасцей, PRP таксама з'яўляецца багатай крыніцай многіх фактараў росту, біямалекул, якія могуць супрацьстаяць шкодным эфектам у запаленых тканінах, кантралюючы абвастрэнне запалення і ствараючы анабалічныя стымулы.Улічваючы гэтыя ўласцівасці, даследчыкі могуць знайсці вялікі патэнцыял у лячэнні розных складаных траўмаў.
2. Цітокіны
Цітокіны ў PRP гуляюць ключавую ролю ў маніпуляцыі працэсамі аднаўлення тканін і рэгуляцыі запаленчых пашкоджанняў.Супрацьзапаленчыя цітокіны - гэта шырокі спектр біяхімічных малекул, якія апасродкуюць провоспалительные цітокіны рэакцыі, у асноўным індукаваныя актываванымі макрофагов.Супрацьзапаленчыя цітокіны ўзаемадзейнічаюць са спецыфічнымі інгібітарамі цітокіны і растваральнымі рэцэптарамі цітокіны для мадуляцыі запалення.Антаганісты рэцэптараў інтэрлейкіну (IL)-1, IL-4, IL-10, IL-11 і IL-13 класіфікуюцца як асноўныя супрацьзапаленчыя цітокіны.У залежнасці ад тыпу раны, некаторыя цітокіны, такія як інтэрферон, інгібіруе лейкемію фактар, TGF-β і IL-6, могуць праяўляць пра- або супрацьзапаленчае дзеянне.TNF-α, IL1 і IL-18 маюць пэўныя рэцэптары цітокіны, якія могуць інгібіраваць провоспалительное дзеянне іншых бялкоў [37].IL-10 з'яўляецца адным з самых магутных супрацьзапаленчых цітокіны, ён можа паніжаць супрацьзапаленчыя цітокіны, такія як IL-1, IL-6 і TNF-α, і ўзмацняць супрацьзапаленчыя цітокіны.Гэтыя механізмы контррэгуляцыі гуляюць важную ролю ў выпрацоўцы і функцыянаванні провоспалительных цітокіны.Акрамя таго, некаторыя цітокіны могуць выклікаць спецыфічныя сігнальныя рэакцыі, якія стымулююць фібрабласты, якія важныя для аднаўлення тканін.Запаленчыя цітокіны TGFβ1, IL-1β, IL-6, IL-13 і IL-33 стымулююць фібрабласты дыферэнцавацца ў миофибробласты і паляпшаюць ECM [38].У сваю чаргу фібрабласты вылучаюць цітокіны TGF-β, IL-1β, IL-33, CXC і CC хемокіны, якія спрыяюць провоспалительным рэакцыям шляхам актывацыі і вярбоўкі імунных клетак, такіх як макрафагі.Гэтыя запаленчыя клеткі выконваюць некалькі роляў у месцы раны, у першую чаргу спрыяючы ачышчэнню раны, а таксама біясінтэзу хемокінаў, метабалітаў і фактараў росту, якія важныя для рэканструкцыі новай тканіны.Такім чынам, цітокіны, якія прысутнічаюць у PRP, гуляюць важную ролю ў стымуляцыі імунных рэакцый, апасродкаваных клеткавым тыпам, спрыяючы дазволу фазы запалення.Фактычна, некаторыя даследчыкі назвалі гэты працэс «рэгенератыўным запаленнем», мяркуючы, што фаза запалення, нягледзячы на неспакой пацыента, з'яўляецца найважнейшым крокам, неабходным для паспяховага завяршэння працэсу аднаўлення тканін, улічваючы эпігенетычныя механізмы, з дапамогай якіх сігналы запалення спрыяюць клеткавым пластычнасць.
3. Фібрына
Трамбацыты нясуць некалькі фактараў, звязаных з фібрыналітычнай сістэмай, якія могуць узмацняць або зніжаць рэгуляцыю фібрыналітычнай рэакцыі.Часовая ўзаемасувязь і адносны ўклад гематалагічных кампанентаў і функцыі трамбацытаў у дэградацыю згустку застаецца праблемай, вартай шырокага абмеркавання ў грамадстве.У літаратуры прадстаўлена шмат даследаванняў, прысвечаных толькі трамбацытаў, якія вядомыя сваёй здольнасцю ўплываць на працэс гаення.Нягледзячы на шматлікія выдатныя даследаванні, іншыя гематалагічныя кампаненты, такія як фактары згортвання крыві і фібрыналітычная сістэма, таксама ўносяць важны ўклад у эфектыўнае залячэнне ран.Па вызначэнні фібрыналіз - гэта складаны біялагічны працэс, які абапіраецца на актывацыю пэўных ферментаў для палягчэння дэградацыі фібрына.Фібрыналітычная рэакцыя была выказана іншымі аўтарамі, што прадукты дэградацыі фібрына (fdp) на самай справе могуць быць малекулярнымі агентамі, адказнымі за стымуляцыю аднаўлення тканін, паслядоўнасць важных біялагічных падзей перад адкладаннем фібрына і выдаленнем з ангіягенезу, што неабходна для гаення ран.Адукацыя згустку пасля траўмы дзейнічае як ахоўны пласт, які абараняе тканіну ад страты крыві, інвазіі мікробных агентаў, а таксама забяспечвае часовую матрыцу, праз якую клеткі могуць міграваць падчас аднаўлення.Згустак з'яўляецца з-за расшчаплення фібрынаген сериновыми протеазами і агрэгацыі трамбацытаў у папярочна-пашытай фібрына фіброзна сеткі.Гэтая рэакцыя ініцыюе полімерызацыю манамераў фібрына, галоўнай падзеі ў адукацыі тромба.Згусткі таксама могуць выступаць у якасці рэзервуараў для цітокіны і фактараў росту, якія вылучаюцца пры дэгрануляцыі актываваных трамбацытаў.Фибринолитическая сістэма жорстка рэгулюецца плазмином і гуляе ключавую ролю ў садзейнічанні міграцыі клетак, біялагічнай даступнасці фактару росту і рэгуляцыі іншых протеазных сістэм, якія ўдзельнічаюць у запаленні і рэгенерацыі тканін.Вядома, што ключавыя кампаненты фібрыналізу, такія як рэцэптар актыватара плазмінагену урокіназы (uPAR) і інгібітар актыватара плазмінагену-1 (PAI-1), экспрэсуюцца ў мезенхімальных ствалавых клетках (МСК), спецыялізаваным тыпе клетак, неабходных для паспяховага гаення ран.
4. Міграцыя клетак
Актывацыя плазминогена праз асацыяцыю uPA-uPAR - гэта працэс, які спрыяе міграцыі запаленчых клетак, паколькі гэта ўзмацняе пазаклеткавы пратэаліз.Паколькі ў uPAR адсутнічаюць трансмембранны і ўнутрыклетачны дамены, для рэгулявання клеткавай міграцыі бялку патрэбныя корецепторы, такія як інтэгрыны і вітрэйны.Акрамя таго, звязванне uPA-uPAR прывяло да павелічэння сродства uPAR да каннексінаў і інтэгрынаў шклопадобнага цела, спрыяючы адгезіі клетак.Інгібітар актыватара плазмінагену-1 (PAI-1), у сваю чаргу, адключае клеткі, разбураючы упар-вітрэін і інтэгрын, калі ён звязваецца з uPA комплексу uPA-упар-інтэгрын на паверхні клеткі. Узаемадзеянне шкляных вокселяў.
У кантэксце рэгенератыўнай медыцыны мезенхімальныя ствалавыя клеткі мабілізуюцца з касцявога мозгу ў кантэксце сур'ёзных пашкоджанняў органаў і, такім чынам, могуць быць знойдзены ў кровазвароце пацыентаў з множнымі пераломамі.Аднак пры пэўных абставінах, такіх як тэрмінальная стадыя нырачнай недастатковасці, тэрмінальная стадыя пячоначнай недастатковасці або падчас пачатку адрыньвання пасля трансплантацыі сэрца, гэтыя клеткі могуць не выяўляцца ў крыві [66].Цікава, што гэтыя мезенхімальныя (стромальных) клеткі-папярэднікі касцявога мозгу чалавека немагчыма выявіць у крыві здаровых людзей [67].Роля uPAR у мабілізацыі мезенхімальных ствалавых клетак касцявога мозгу таксама была прапанавана раней, падобна таму, што адбываецца пры мабілізацыі гемопоэтических ствалавых клетак (HSC).Варабанені і інш.Вынікі паказалі, што выкарыстанне гранулоцитарного колониестимулирующего фактару ў мышэй з дэфіцытам uPAR выклікала адмову МСК, зноў узмацняючы дапаможную ролю фібрыналітычнай сістэмы ў клеткавай міграцыі.Далейшыя даследаванні таксама паказалі, што рэцэптары uPA, замацаваныя на гліказілфасфатыдыліназітол, рэгулююць адгезію, міграцыю, праліферацыю і дыферэнцыяцыю шляхам актывацыі пэўных ўнутрыклеткавых сігнальных шляхоў, а менавіта: фасфатыдыліназітол 4,5-бісфасфат 3-кіназа/Akt і сігнальныя шляхі ERK1/2, якія спрыяюць выжыванню. і кіназа адгезіі (FAK).
МСК прадэманстравалі далейшае значэнне ў кантэксце гаення ран.Напрыклад, мышы з дэфіцытам плазмінагену дэманстравалі сур'ёзныя затрымкі гаення ран, што сведчыць аб тым, што плазмін крытычна ўцягнуты ў гэты працэс.У людзей страта плазміну таксама можа прывесці да ўскладненняў пры гаенні ран.Парушэнне крывацёку можа значна тармазіць рэгенерацыю тканін, што тлумачыць, чаму гэтыя рэгенератыўныя працэсы больш складаныя ў пацыентаў з дыябетам.
5. Манацыты і сістэмы рэгенерацыі
Па дадзеных літаратуры, існуе шмат дыскусій аб ролі манацытаў у гаенні ран.Макрафагі ў асноўным паходзяць з манацытаў крыві і гуляюць важную ролю ў рэгенератыўнай медыцыне [81].Паколькі нейтрофілов сакрэтуюць IL-4, IL-1, IL-6 і TNF-α, гэтыя клеткі звычайна пранікаюць у месца раны прыкладна праз 24-48 гадзін пасля траўмы.Трамбацыты вызваляюць трамбін і фактар трамбацытаў 4 (PF4), два хемокіны, якія спрыяюць вярбоўцы манацытаў і іх дыферэнцыяцыі ў макрафагі і дендрытныя клеткі.Яркай асаблівасцю макрофагов з'яўляецца іх пластычнасць, г.зн. іх здольнасць пераключаць фенатып і трансдыферэнцыявацца ў іншыя тыпы клетак, такія як эндотелиальные клеткі, якія пасля дэманструюць розныя функцыі ў адказ на розныя біяхімічныя стымулы ў мікраасяроддзі раны.Запаленчыя клеткі выяўляюць два асноўных фенатыпу, M1 або M2, у залежнасці ад лакальнага малекулярнага сігналу, які з'яўляецца крыніцай стымулу.Макрафагі M1 індукуюцца мікробнымі агентамі і, такім чынам, аказваюць больш провоспалительное дзеянне.Наадварот, макрафагі М2 звычайна ўтвараюцца ў адказ тыпу 2 і валодаюць супрацьзапаленчымі ўласцівасцямі, якія звычайна характарызуюцца павелічэннем IL-4, IL-5, IL-9 і IL-13.Ён таксама ўдзельнічае ў аднаўленні тканін праз выпрацоўку фактараў росту.Пераход ад ізаформ M1 да M2 у значнай ступені абумоўлены пазнейшымі стадыямі гаення ран, дзе макрафагі M1 запускаюць апоптоз нейтрофілов і ініцыююць ачышчэнне гэтых клетак).Фагацытоз нейтрофілов актывуе ланцужок падзей, у якіх выпрацоўка цітокіны адключаецца, палярызуючы макрафагі і вызваляючы TGF-β1.Гэты фактар росту з'яўляецца ключавым рэгулятарам дыферэнцыявання миофибробластов і скарачэння раны, дазваляючы ліквідаваць запаленне і ініцыяваць фазу пролиферации ў каскадзе гаення [57].Іншым блізкім бялком, які ўдзельнічае ў клеткавых працэсах, з'яўляецца серын (SG).Было ўстаноўлена, што гэты гранулан, які вылучаецца крывятворнымі клеткамі, неабходны для захоўвання сакрэтаваных бялкоў у спецыфічных імунных клетках, такіх як гладкія клеткі, нейтрофілов і цітотоксіческой Т-лімфацыты.У той час як многія негемопоэтические клеткі таксама сінтэзуюць серотонін, усе запаленчыя клеткі вырабляюць вялікую колькасць гэтага бялку і захоўваюць яго ў гранулах для далейшага ўзаемадзеяння з іншымі медыятарамі запалення, уключаючы пратэазы, цітокіны, хемокіны і фактар росту.Адмоўна зараджаныя глікозамінагліканавыя (GAG) ланцугі ў SG, па-відаць, маюць вырашальнае значэнне для гамеастазу сакраторных гранул, паколькі яны могуць звязвацца з істотна зараджанымі кампанентамі гранул і садзейнічаць іх захоўванню спецыфічным чынам для клетак, бялкоў і GAG-ланцугоў.Што тычыцца іх удзелу ў PRP, Woulfe і яго калегі раней паказалі, што дэфіцыт SG цесна звязаны са зменай марфалогіі трамбацытаў;дэфекты захоўвання трамбацытаў фактару 4, бэта-трамглабуліну і PDGF у трамбацытаў;дрэнная агрэгацыя і сакрэцыя трамбацытаў in vitro і трамбоз in vivo дэфекты формы.Такім чынам, даследчыкі прыйшлі да высновы, што гэты пратэаглікан, здаецца, з'яўляецца галоўным рэгулятарам трамбозу.
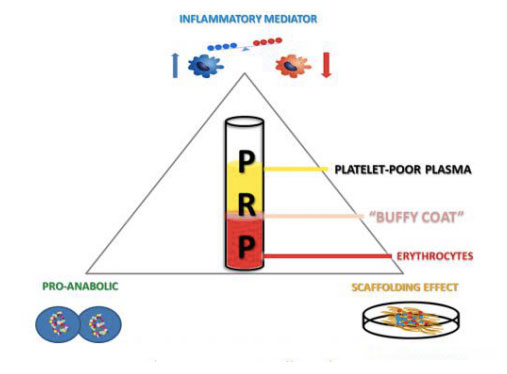
Прадукты, багатыя трамбацытамі, можна атрымаць шляхам збору і цэнтрыфугавання суцэльнай крыві чалавека, падзелу сумесі на розныя пласты, якія змяшчаюць плазму, трамбацыты, лейкацыты і лейкацыты.Калі канцэнтрацыя трамбацытаў вышэй базальных значэнняў, рост костак і мяккіх тканін можа быць паскораны з мінімальнымі пабочнымі эфектамі.Прымяненне аутологичных прадуктаў PRP - гэта адносна новая біятэхналогія, якая працягвае паказваць шматспадзеўныя вынікі ў стымуляцыі і палепшаным гаенні розных пашкоджанняў тканін.Эфектыўнасць гэтага альтэрнатыўнага тэрапеўтычнага падыходу можна звязаць з мясцовай дастаўкай шырокага спектру фактараў росту і бялкоў, якія імітуюць і падтрымліваюць фізіялагічныя працэсы гаення ран і аднаўлення тканін.Акрамя таго, фібрыналітычная сістэма відавочна аказвае важны ўплыў на агульнае аднаўленне тканін.У дадатак да сваёй здольнасці змяняць клеткавы набор клетак запалення і мезенхімальных ствалавых клетак, ён мадулюе пратэялітычную актыўнасць у зонах гаення ран і падчас рэгенерацыі мезадэрмальных тканін, уключаючы косці, храсткі і мышцы, і таму з'яўляецца ключавым кампанентам медыцыны апорна-рухальнага апарата.
Паскарэнне гаення з'яўляецца вельмі запатрабаванай мэтай многіх спецыялістаў у галіне медыцыны, і PRP уяўляе сабой пазітыўны біялагічны інструмент, які працягвае прапаноўваць перспектыўныя распрацоўкі ў стымуляцыі і добра скаардынаваным тандэме рэгенератыўных падзей.Аднак, паколькі гэты тэрапеўтычны інструмент застаецца складаным, асабліва з-за таго, што ён вызваляе мноства біялагічна актыўных фактараў і іх розныя механізмы ўзаемадзеяння і сігнальныя эфекты, патрабуюцца далейшыя даследаванні.
(Змесціва гэтага артыкула перадрукавана, і мы не даем ніякіх відавочных або пэўных гарантый на дакладнасць, надзейнасць або паўнату змесціва, якое змяшчаецца ў гэтым артыкуле, і не нясем адказнасці за меркаванні гэтага артыкула, калі ласка, зразумейце.)
Час публікацыі: 19 ліпеня 2022 г